
El presente documento es una recopilación de excelentes libros que narran de una manera agradable los descubrimientos realizados por los científicos en los últimos 300 años.
He procurado hacer el mínimo cambio a la narración de los autores: el doctor Carl Sagan en su libro Cosmos nos hace viajar a través del sistema solar, el doctor Marcelino García-Junco en La magia de los sentidos nos enseña mediante una didáctica incomparable. Por ultimo, el doctor William Cecil Dampier en Historia de la ciencia y de sus relaciones con la filosofía y la religión nos presenta en forma sistemática y objetiva los descubrimientos hechos por el ser humano.
Si esta recopilación logra despertar la curiosidad para conocer más acerca no sólo de la espectrometría sino de todas las ciencias, habré logrado mi objetivo.
Historia de la espectrometría
La distinción entre la esfera celeste y la terrestre, que perduró durante toda la edad media, fue desmentida por Galileo y Newton, cuando demostraron que las leyes mecánicas de la caída de los cuerpos –en forma experi-mental- eran aplicables a todo el sistema solar.
Para completar lo afirmado se debía probar que los elementos químicos que componen las cosas terrestres, existían también en la sustancia del Sol, los planetas y las estrellas. Este anhelo parecía inaccesible para el ser humano; sin embargo a mediados del siglo XIX se solucionó científicamente.
Isaac Newton descubre el espectro

En el espectro coloreado generado a partir de la luz blanca, él contempló “la mas sorprendente composi-ción…de blancura”. Newton no era el primero en observar la luz blanca dividida de tan hermosa manera, pero sí en tener la idea de que la luz está compuesta de diversos rayos que se desvían en proporción diferente al pasar a través del cristal. Además, demostró que si hacia pasar los rayos refractados a través de un segundo prisma, el haz resultante volvería a ser blanco.
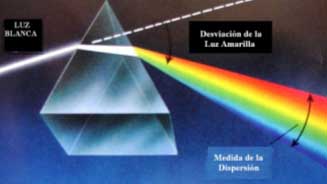
Descomposición de la luz en un prisma
Ahora los físicos saben que tal refracción ocurre porque cada color de luz, o longitud de onda, se mueve a diferente velocidad a través del cristal. El arco iris por ejemplo, es un espectro que se forma cuando la luz blanca es refractada por pequeñas gotitas de agua suspendidas en el aire.
Newton indicó que las franjas de colores generadas por el paso de los rayos del Sol a través de un prisma de cristal, se debían a la descomposición de la luz blanca en los elementos físicos simples.
En 1802 Wollaston descubrió que este espectro luminoso se hallaba cruzado por una serie de rayas oscuras. Joseph Fraunhofer nació en Straubing, Bavie-ra 1787 y murió en Munich en 1826. Fraunhofer en 1814 volvió a observar tales “rayas”, y aumentando la dispersión a través de diverso prismas, las clasificó cuidadosamente.
Por otra parte, se comprobó que la luz proveniente de llamas coloreadas con sales o metales (apreciadas por primera vez por Melvil en 1752) originaba un espectro con líneas brillantes sobre un fondo oscuro, y Herschel, en 1823 expuso la idea de que tales líneas podían ser empleadas para acusar la presencia de metales. La consecuencia de todo esto fue la verificación de una serie de observaciones en las que se marcó y anotó detalladamente la posición de las rayas espectrales.
Nace el análisis espectral
Roberto Guillermo Bunsen nació el 31 de marzo de 1811 en Gotinga, y murió en Heidelberg el 16 de agosto de 1899. Gustavo Roberto Kirchhoff nació en Köenigsberg el 12 de marzo de 1824 y murió el 16 de octubre de 1887 en Berlín; ambos son los creadores del análisis espectral.
En 1849 MichelFoucault, (que había nacido en París en 1819 y falleció en la misma ciudad en 1868), examinó el espectro de la luz generada por un arco voltaico saltando entre polos de carbón y observó una doble línea brillante cuyo color iba del amarillo al anaranjado, y coincidía exactamente con la doble raya oscura, a la que Foucault llamó D. Así supo que cuando se hacía pasar la luz del Sol a través del arco, la línea D aparecía más oscura que de ordinario, y cuando la luz de uno de los carbones –que por si misma engendraba un espectro brillante y continuo sin rayas negras- se hacía pasar a través del arco, las líneas D aparecían. “Así, el arco se nos ofrece como un medio que emite por sí mismo los rayos D, y que al mismo tiempo los absorbe cuando tienen otra procedencia”, decía Foucault.
Desconocedores de los experimentos de Foucault, Bunsen y Kirchhoff hicieron pasar una luz de calcio –que originaba un espectro continuo- por una llama de alcohol, en la que se vertió sal común (cloruro de sodio), y descubrieron las rayas D de Fraunhofer; repitieron el experimento con el litio en la llama de un mechero Bunsen de gas y obtuvieron una raya oscura que no aparecía en el espectro del Sol. De estos ensayos dedujeron que el sodio si existía en la atmósfera del Sol, pero que el litio no, o al menos no en cantidades apreciables.
La ciencia se vale del “análisis espectral” para demostrar la existencia de tales o cuales elementos químicos en los demás planetas y en las estrellas, dicho análisis se funda debido a que los elementos químicos emiten luz de colores cuando se encuentran en estado incandescente.
Seis años después, el estadounidense David Alter describió los espectros del hidrógeno y otros gases. Entre 1855 y 1863 Von Bunsen y Kirchhoff realizaron una serie de experimentos acerca de la acción química de la luz, y en 1859 proyectaron los primeros métodos exactos de análisis espectral que permitieron descubrir los elementos químicos mediante sus espectros, aun cuando aquéllos se ofrecieran en cantidades minúsculas. Así descubrieron dos nuevos elementos: el cesio y el rubidio.
Un viaje por las estrellas
El rayo de luz atraviesa el espacio a una velocidad aproximadamente de los 300 mil kilómetros por segundo (2.99792458·108 m·s-1), es el mensajero que nos trae esa información. Mediante el análisis espectral se averiguó la composición de los cuerpos celestes alejados de nosotros miles de años luz (en el sistema métrico decimal, el año luz es equivalente a 9 billones, 460 mil 800 millones de kilómetros (9.4608·1015 m).
En 1844 el filósofo Auguste Comte buscó un ejemplo de un tipo de conocimiento que estaría siempre oculto, así escogió la composición de las estrellas y de los planetas lejanos. Pensó que nunca los podríamos visitar físicamente, y que al no tener a la mano alguna muestra de ellos, jamás conoceríamos su composición. A tres años de la muerte de Comte, se descubrió que un espectro puede ser utilizado para determinar la composición química de los objetos distantes.
Diversas moléculas o elementos químicos absorben diferentes frecuencias o colores de luz, en ocasiones en la zona visible y otras en algún otro lugar del espectro. En el espectro de la atmósfera de un planeta, una línea oscura aislada representa una imagen de la hendidura en la que falta luz: la absorción de luz solar durante su breve paso a través del aire de otro mundo. Cada tipo de línea está compuesto por una clase particular de moléculas o átomos, y cada sustancia tiene su forma espectral característica.
Los gases en el planeta Venus pueden ser identificados desde la Tierra, a 60 millones de kilómetros de distancia; incluso podemos adivinar la composición del Sol, en el que se descubrió por vez primera el helio (nombrado a partir de Helios, el dios griego del Sol), así como la composición de las estrellas magnéticas Ă ricas en europio, y también galaxias lejanas analizadas a partir de la luz que envían colectivamente los cien mil millones de estrellas.
La astronomía espectroscópica es una técnica casi mágica, a Carl Sagan y a muchos otros nos asombra. Auguste Comte escogió un ejemplo especialmente inoportuno. Dicha técnica adquirió un gran auge merced a los trabajos de Huggins, Janssen y Lockyer; éste último observó en 1878 una raya oscura en el espectro de la cromosfera solar, la cual no coincidía con alguna raya conocida de los espectros terrestres. Predijo junto con Franland, la existencia de un elemento desconocido en el Sol: el helio, descubierto 17 años después, en 1895 por Ramsay en el mineral clavita.[1]
En las estrellas blancas, cuya temperatura superficial se aprecia en más de 12 mil grados Celsius, como la alfa (a) de Cisne, la gamma (g) de Casiopea, La Vega de Lira, Sirio y Rigel –por otro nombre beta (b) de Orión-, se ha demostrado que existen el hidrógeno, el helio, el calcio y el hierro.
Las estrellas amarillas (como nuestro Sol) que tienen una temperatura superficial alrededor de 6 mil grados Celsius, el análisis espectral indica la existencia de por lo menos 35 elementos químicos muy conocidos en la Tierra: sodio, cromo, cobre, estroncio, titanio, molibdeno, berilio, escandio, manganeso, plata, cadmio, germanio,, rutenio, neodimio, hierro, magnesio,, bario, circonio, paladio, itrio, carbono, cobalto, calcio, estaño, lantano, níquel, erbio, plomo, cerio, silicio, zinc, niobio, vanadio y boro.
En estrellas rojas –como la de Orión, la de Hércules, la de Pegaso-, y soles que se encuentran a temperaturas relativamente bajas (entre los 2,500 y 3,000 grados Celsius), se han identificado otros elementos y compuestos químicos conocidos en la Tierra que son estables a esas temperaturas.
El espectro solar muestra, entre las cien mil rayas que se han observado, algunas que pertenecen a un elemento químico que nunca se ha encontrado en la Tierra y al que se le llamó coronio.
En las nebulosas lejanas de Orión, del Cisne y de las Pléyades, el análisis espectral señala la existencia del helio, del hidrógeno, y de otros elementos desconocidos en la Tierra (de existencia muy poco probable), que los astrónomos denominan nebulio y asterio.
Los conocimientos adquiridos en los últimos años, en relación con los nuevos elementos artificiales llamados transuránicos, (once hasta la fecha) tal vez podrán explicar lo concerniente a los elementos dudosos: coronio, nebulio y asterio. La cauda de los cometas produce los espectros característicos de hidrógeno y compuestos químicos conocidos, como el bióxido de carbono, los hidrocarburos y el cianógeno.
La visibilidad de las nebulosas es posible debido al espesor de millones de kilómetros que alcanzan, y a la presencia de ciertos fenómenos eléctricos de la misma naturaleza, de los que se observan en los tubos de Rayos X.
Las nebulosas son huellas materiales que han quedado como residuo, al acumularse la materia cósmica dispersa por procedimientos físicos sencillos. Debido a algunas anomalías en los espectros observados, se creyó que las nebulosas se encontraban a temperaturas altísimas y que, debido a tales condiciones térmicas, los elementos químicos se encontraban disociados y que éstos formaron a los mundos en un principio. Así, se consideró a las nebulosas como la primera esencia cósmica. Sin embargo, ahora se confirma lo contrario: la temperatura de las nebulosas casi coincide con la de los espacios siderales vacíos, que es el límite de la cinética material y que se halla a menos 273 grados Celsius, casi el cero absoluto.
La dilución de los componentes de las nebulosas sobrepasa toda capacidad imaginativa: es miles de veces más grande, que los más intensos enrarecimientos que se pueden crear en los laboratorios.
Por otra parte, en las llamadas auroras boreales y australes (causadas por las tempestades eléctricas que suceden a más de 100 kilómetros sobre la superficie de los mares), el análisis espectral delata la existencia de hidrógeno, helio, argón, neón y nitrógeno.
La teoría de Fraunhofer acerca de las rayas espectrales parece que fue esclarecida por George Gabriel Stokes (1819-1903) en las conferencias pronunciadas en Cambridge, aunque su modestia característica impidió que tales ideas alcanzaran más publicidad: Todo sistema mecánico absorberá la energía que manifieste a un ritmo unísono con sus vibraciones naturales, del mismo modo que el columpio de un niño es propulsado por pequeños impulsos que coinciden con el periodo de la oscilación de aquél.
Así, las moléculas de los vapores que forman la corona del Sol absorberán la energía de aquellos rayos particulares provenientes del núcleo más caliente, y cuyo periodo oscilatorio armonice con el de aquellas. De esta forma, la luz que atraviese dicha corona quedará privada de la luz o color corres-pondiente a aquella frecuencia de vibración, y el resultado será una raya negra visible en el espectro.
El Espectro electromagnético
La primera pista real sobre la naturaleza del planeta Venus se obtuvo trabajando con un prisma de vidrio o una superficie plana, llamada red de difracción, en la que se graba un conjunto de líneas finas y espaciadas.
Cuando un haz intenso de luz blanca y corriente pasa a través de una hendidura estrecha y después atraviesa un prisma o una red, se esparce formando un arco iris de colores: un espectro, éste se extiende desde las frecuencias altas de la luz visible hasta las bajas; es decir desde el violeta, pasando por el azul, verde, amarillo, anaranjado y finalmente el rojo.
Como estos colores pueden verse, se le denominó espectro de luz visible, pero hay mucha más luz que la del pequeño segmento del espectro que alcanzamos a ver.
En frecuencias más altas, con respecto al violeta, existe una parte del espectro llamada ultravioleta, que es un tipo de luz perfectamente real, portadora de muerte para los microbios. Para nosotros es invisible, pero la detectan con facilidad los abejorros y las células foto-eléctricas.
Entre tanto, la identificación de la naturaleza física de la luz y del calor radiante ya había sido demostrada plenamente. En 1800, William Herschel (Hannover 1738 – Slough 1822), puso de manifiesto que al colocar un termómetro en el espectro solar se observan efectos caloríficos que se extienden más allá de la luz roja visible. Poco después, Ritter encontró rayos más allá del violeta visible, que oscurecían el nitrato de plata y cuya acción fotográfica fue descubierta por Scheele en 1777.
Entre 1830 y 1840 Melloni comprobó que el calor invisible mostraba propiedades similares a las de la luz en cuanto a los fenómenos de reflexión, polarización e interferencia.
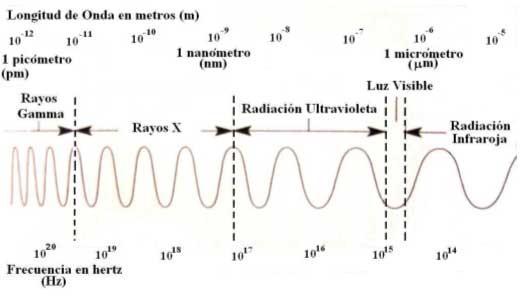
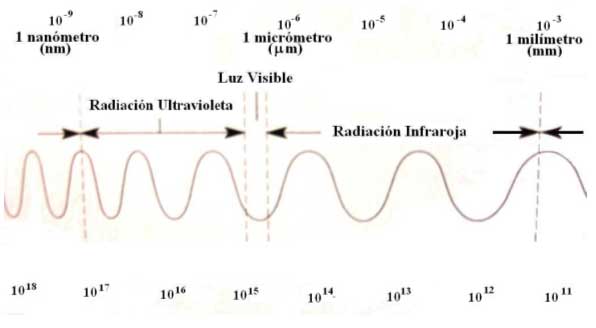
En el espectro electromagnético, de la longitud de onda más corta (rayos gamma) hasta la más larga (ondas de radio), la longitud de onda de la luz se calcula en Ångtröms (Å es igual a 10-10m), nanómetros (nm es igual 10-9m), micrómetros (µm es igual a 10-6m), centímetros (cm es igual a 10-2m) y metros (m).
Después del ultravioleta está la parte de rayos X del espectro, y le siguen los rayos gamma. En las frecuen-cias bajas, del lado del rojo, se encuentra la parte infrarroja del espectro. Al colocar un termómetro sensible en una zona situada más allá del rojo (oscuridad ante nuestra vista), se descubrió que la temperatura del termómetro aumentó y detectaba luz sobre él, aunque fuera invisible a nuestros ojos.
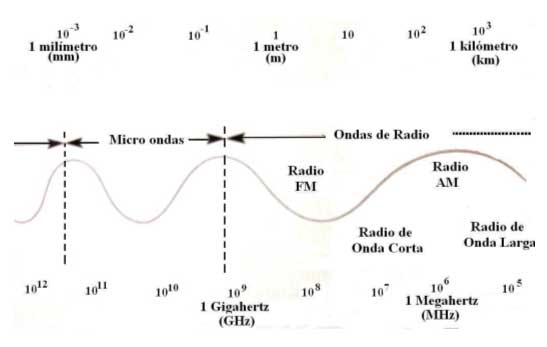
Las serpientes de cascabel y los semiconductores contaminados detectan perfectamente la radiación infrarroja. Después del infrarrojo está la región espectral de las ondas de radio.
Los trabajos de William Crookes
En 1859, año de la fundación del Chemical News, el mundillo científico se conmovió con la noticia de la invención de la nueva forma de análisis químico: el análisis espectral, creado por Kirchhoff y Bunsen, entre cuyos primeros éxitos se cuenta el descubrimiento del cesio y del rubidio.
William Crookes aplicó el novedoso método de análisis a los residuos que le quedaron de sus investigaciones en relación con el selenio, y al llevar a la llama del espectroscopio una porción de los residuos del selenio, observó una raya verde que no correspondía a ninguno de los espectros de los elementos químicos conocidos en esa época. Dicha observación le hizo suponer la existencia de un nuevo elemento químico: el talio (1861), nombre que le pusiera Crookes debido a la línea verde característica de su espectro (tallos, rama verde).
En su empeño de aumentar la sensibilidad de la balanza con la que determinaba el peso atómico del talio, Crookes hace su segundo descubrimiento en 1874: la atracción y repulsión causadas por radiación, fenómeno al que llamó fuerzas radiométricas. Esas investigaciones le llevaron al estudio de los rayos catódicos que produjo con gran pureza, y cuyos resultados fueron una serie de ingeniosos aparatos –que aun se usan en todas las escuelas del mundo con fines pedagógicos- para demostrar el carácter material de ellos, y el descubrimiento de lo que llamó Crookes cuarto estado de la materia o estado radiante.
Parte de un discurso de Crookes en 1879 dice “…nos encontramos frente a un nuevo estado de agregación de la materia, tan distante del estado gaseoso como del líquido. Al estudiar este cuarto estado de la materia, nos parece tener en las manos y dentro del campo de nuestra experiencia a las pequeñas partículas indivisibles que, con buenos fundamentos, podemos considerar que forman la sustancia física del Universo. Hemos visto que en algunas de sus propiedades, la materia radiante es tan material como lo puede ser la masa, mientras que otras propiedades coinciden con el carácter de energía radiante. Hemos tocado efectivamente el territorio en que la fuerza y la materia parecen transformarse una en otra, y viceversa, territorio de las sombras que separan a lo conocido de lo desconocido, y que para mí siempre ha tenido una gran fascinación. Pienso que los grandes problemas científicos del futuro encontrarán resolución en esta región límite y más adelante aún. Aquí tal parece, se hallan las últimas realidades”.
Energía Radiante
La equivalencia entre el poder emisor y el poder absorbente fue extendida al calor radiante por Kirchhoff y Stewart, especialmente.
Se descubrió también que un cuerpo negro que absorbe a todas las radiaciones al calentarse, emite radiaciones de todas las longitudes de onda, y Provost en su teoría de los intercambios (1792) hace notar que todos los cuerpos irradian calor, aunque cuando existe equilibrio, reciben mucho más de lo que ceden.
Maxwell expuso teóricamente su creencia de que la radiación debía ejercer una cierta presión sobre la superficie en la cual actuaba; esta presión fue com-probada posteriormente en forma experimental.
En 1875 Bartoli sugirió la idea que la existencia de esta presión permite imaginar un espacio lleno con tales radiaciones, la presión podía obrar como el cilindro de una máquina termodinámica teórica. En 1884, Bolzmann estableció la ley en la cual la radiación completa de un cuerpo negro aumenta con la cuarta potencia de la temperatura absoluta, o sea R = aT4. Esta ley ya había sido planteada empíricamente por Stefan en 1879.
Este resultado revestía utilidad no sólo desde el punto de vista de la teoría de la radiación, sino también serviría para medir las temperaturas de los hornos y aun de las superficies del Sol y las estrellas debido a la observación de la energía calorífica que proporcionan. Cuando la temperatura se eleva, no solo la radiación total aumenta, sino que la energía máxima emitida es desplazada hacia las longitudes de onda más cortas.
El 14 de diciembre de 1900, Max Planck presenta los fundamentos teóricos de su fórmula adecuada solamente para las frecuencias bajas, y establece la hipótesis de que tanto la emisión como la absorción sólo pueden efectuarse de un modo brusco, de manera que, la energía emitida o absorbida cada vez, sea igual a un múltiplo entero de una magnitud elemental e (épsilon) llamada quantum de energía
(e = hv).
Además encontró que los cuantos de energía son proporcionales a la frecuencia v, y determinó correc-tamente la magnitud de la constante de proporcióna-lidad h que ahora se conoce como la constante de Planck
h = 6.624·10-27 erg · s = 6.626076·10-34 J · s.
Aunque este adelanto tendría consecuencias de largo alcance –pues finalmente condujo al desarrollo de la mecánica cuántica-, su importancia no fue obvia inmediatamente. A cinco años del descubrimiento de Planck, Albert Einstein aplicó por vez primera el concepto cuántico en su teoría del efecto fotoeléctrico, y estableció la idea de cuantos de luz, como forma moderna de los corpúsculos de luz de Newton.
Más tarde, en 1913 Bohr introdujo su teoría cuántica del espectro atómico, la cual condujo a su vez, a la fundación de la mecánica cuántica. Desde entonces, el concepto de luz adquirió el aspecto de una personalidad dividida. La radiación debía considerarse algunas veces como onda y otras como partícula, de acuerdo con la naturaleza de su interacción con la materia. Naturalmente, ello era odioso para los contemporáneos de Planck, y él mismo hizo varios intentos para reconciliar los dos puntos de vista: el ondulatorio y el corpuscular. Sin embargo, ni sus intentos ni los de otros tuvieron éxito y los físicos han aceptado la naturaleza dual de la radiación como parte de la vida.
Bibliografía
- Dampier, William Cecil (1929)
A history of science and its relations with philosophy & religión. Versión en español traducida por Luís Bravo Gala y Manuel Pérez Urruti. Editorial Galatea. Higinio Arias Ursay. Manuel Gutiérrez Nájera 179, México, Distrito federal. - García-Junco, Marcelino (1960)
La magia de los sentidos. Compañía Editorial Continental, S.A. Calzada de Tlalpan 4620, México 22, Distrito Federal. - Sagan, Carl (1980)
Cosmos. Editorial Planeta, S.A. Córcega, 273-277, Barcelona-8, España. - Simón, Iván (1964)
Infrared radiation. Versión al español de María Teresa Toral y Francisco Medina Nicolau. Editoral Reverte Mexicana, S.A. Pánuco 141-A. México 5, Distrito Federal.
Wilson, Mitchell (1964) - Energía. Colección Científica de LIFE en español. Offset Multicolor, S.A. Calzada de la Viga 1332, México, Distrito Federal
[1] Chemical Society Trans., 1895, pág. 1107.




Artículos Relacionados: