La densidad del Agua
El planeta Tierra se encuentra a una distancia promedio de 149.5 millones de kilómetros del Sol; distancia casi ideal para permitir que la energía solar sobre la molécula del agua en la superficie terráquea, se encuentre en estado líquido, sólido o vapor, es decir se pueda congelar, derretir, evaporar o condensar. Las condiciones anteriores se deben a las extraordinarias cualidades de la molécula de agua, las cuales pasan inadvertidas. En su forma más simple, el agua está compuesta por dos átomos de hidrógeno y un átomo oxígeno. Su formula es H2O.
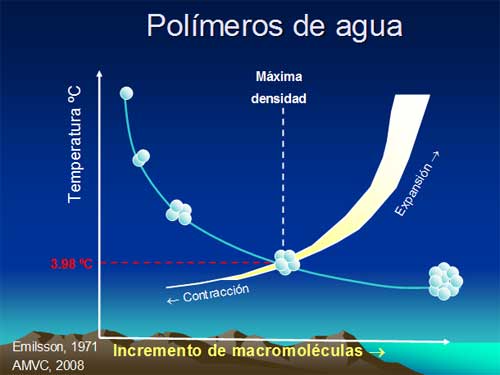
El agua forma macromoléculas, también llamados polímeros, debido al puente de hidrógeno. La formación y destrucción de las macromoléculas de agua en su estado líquido, es la clave de su comportamiento tan especial.
A una atmósfera estándar, el agua a 3.98ºC tiene una densidad de un gramo por centímetro cúbico, o sea su máxima densidad. Por otro lado, el agua a cero grados celsius es de 0.9999 gramos por centímetro cúbico, sin embargo el hielo a cero grados celsius es de 0.9168 gramos por centímetro cúbico.
Los polímeros del agua
El agua en estado líquido, tiene dos efectos que se contraponen con la variación de la temperatura, es decir, con la variación de la energía cinética interna. En el primero, el líquido se contrae a bajas temperaturas, pero se expande a mayores temperaturas; en el segundo, se forman macromoléculas a bajas tempe-raturas, las cuales se disocian en altas temperaturas.
Las moléculas ínter ligadas en aglo-meraciones, que consiguen el equilibrio electroestático se llaman polímeros, o sea las macromoléculas. El agua se evapora a 100ºC, en forma similar el heptano (C7H16) se evapora a 98ºC, la cual es una macromolécula similar en tamaño al polímero del agua.
La energía interna y el agua
La energía interna es una propiedad termodinámica de las substancias, en este caso del agua, la cual incluye la energía cinética interna en las partículas, es decir su movimiento individual; por otro lado la interacción de las energías entre las partículas, su enlace, corresponde a la energía potencial interna.
Un cambio en energía interna durante un proceso, es la diferencia entre el calor transferido al sistema y el trabajo desarro-llado por el mismo.
Una caloría se define como:
“la cantidad de energía que se necesita para elevar un gramo de agua un grado celsius, de 14.5 ºC a 15.5 ºC, a la presión de una atmósfera estándar”. Corresponde a 4.185 joules.
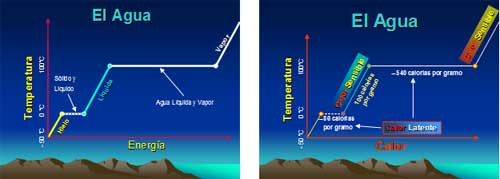
El efecto del cambio de temperatura en el agua corresponde al cambio de energía cinética interna, el cual se conoce como calor sensible; al incrementarle una caloría al agua, aumenta la temperatura un grado celsius.
Por otro lado, las fuerzas eléctricas, magnéticas y de gravedad actúan entre las moléculas, su enlace y agrupación corresponde a la energía potencial interna, llamada calor latente.
Son necesarias aproximadamente 80 calorías, en el agua, para pasar de estado sólido a estado líquido. De la misma manera son necesarias aproximadamente 540 calorías para pasar de estado líquido a estado gaseoso.
Diferentes fases del agua
El agua puede estar en estado sólido, el cual tiene un orden interno fijo, e interacciones muy fuertes, con un volumen determinado. De la misma manera, el agua puede estar en estado líquido, con un orden interno fijo no muy severo, pero con interacciones muy fuertes; como líquido, puede tomar la forma específica de un reservorio, ocupar un volumen y definir una superficie. A su vez, el agua como gas, no tiene un orden interno y es gobernado por interacciones internas muy débiles, adapta y ocupa el volumen totalmente.
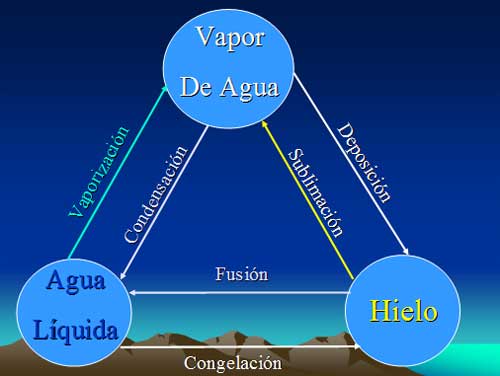
Pasar de estado sólido a estado líquido se llama fusión, de estado líquido a estado sólido se llama congelación. También, de estado líquido a estado gaseoso recibe el nombre de vaporización, y viceversa de estado gaseoso a estado líquido, condensa-ción. Así mismo, se da el caso de pasar de sólido a gas se llama sublimación, y de gas a sólido recibe el nombre se deposición.
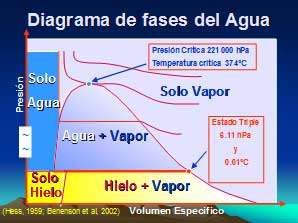
Diagramas termodinámicos del agua
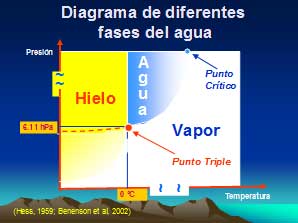
El agua en termodinámica, se puede analizar con diferentes parámetros, presión-temperatura, donde se identifica el punto triple, el cual corresponde al punto donde el agua es sólido, líquido y vapor. Este punto tiene valores de 610.6 pascales (Pa) de presión (6.11 milibares o hectoPascales [hPa] en meteorología), y de 0.01ºC de temperatura.
También se puede analizar con los parámetros presión-volumen específico, donde se observa mejor el punto crítico; este punto corresponde a la isoterma crítica donde la presión deja de incrementarse y empieza a decrecer, en función al incremento del volumen específico. Sus valores son 2.21 ·107 Pa y de 374 ºC.
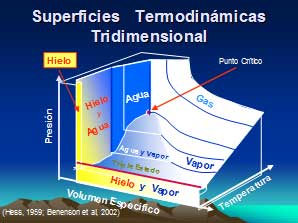
Un diagrama tridimensional de fases presión–temperatura-volumen especifico, proyecta los planos de p-t y de p-v respectivamente. La presión en función de la temperatura no depende del volu-men. Un cambio en el volumen del vapor únicamente afecta a la cantidad de vapor.
Composición del aire y la humedad
El aire en la atmósfera terrestre está compuesta de varios gases, los principales son el Nitrógeno (N2) con un 78.00%, el Oxígeno (O2) con un 20.95%, el Argón (Ar) con un 0.93% y el Bióxido de Carbono (CO2) con un 0.033%. Otros gases solo se encuentran en forma de vestigios.
Sin embargo, el vapor de agua (H2O) varía de 0 a 4%, siendo uno de los compo-nentes más importantes de la atmósfera. La cantidad del vapor de agua en la atmósfera varía día con día y de lugar en lugar. Ésta variabilidad y el movimiento del agua en sus tres fases, es la razón fundamental de muchos aspectos del Estado del Tiempo, incluyendo el cambio de peso del aire.
La humedad es a una cantidad de vapor de agua en el aire.
Definiciones:
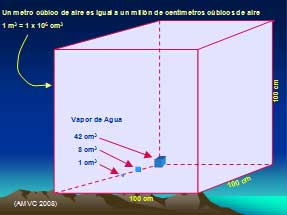
Humedad Absoluta Número de gramos de vapor de agua que contiene un metro cúbico de aire.
Humedad Especifica Cantidad de gramos de agua en un kilogramo de aire húmedo.
Humedad Relativa Relación entre la presión efectiva del vapor de agua y la presión máxima.
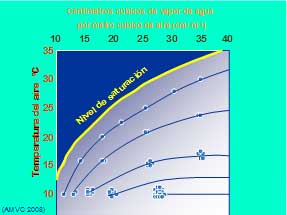
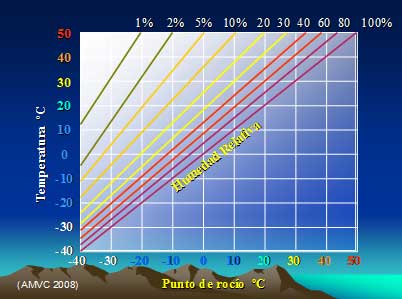
Saturación del Vapor de Agua
Índice de Calor
Cuando nuestros cuerpos se calientan nosotros podemos refréscanos al sudar. No es el sudar lo que nos refresca sino la evaporación del sudor. Si el aire tiene mucha humedad, o sea un valor alto de presión de vapor del agua, entonces disminuye la evaporación. Este impe-dimento hace a nuestro cuerpo no tenga la habilidad de mantener una temperatura casi constante del cuerpo. Esta es la razón por la cual sentimos que el calor no sea nada agradable, son días muy bochornosos.
Como cualquier máquina sin una ventilación apropiada…
Nos sobrecalentamos.
Las personas con alguna actividad física, expuestas a un calor de verano intenso y humedad, hacen que sus cuer-pos estén expuestos a un sobrecalen-tamiento, al punto que pueden desfallecer y morir. Esto se llama golpe de calor.
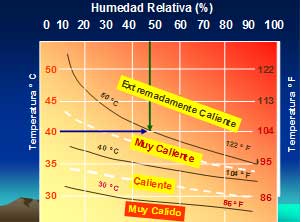
El Índice de Calor o Temperatura Aparente indica el calor que se siente. Se expresa en función de la temperatura y de la humedad relativa.
Índice de Calor
La cantidad de humedad relativa en la atmósfera también afecta la capa-cidad para tener mayor evaporación. Con una misma presión y temperatura, a medida que aumenta la humedad relativa, disminuye la evaporación del agua. Este es un factor primordial para todas las personas, debido a que un valor alto de humedad, hace que la transpiración sea menor, es decir, sudar se vuelve más ineficiente para remover el calor por evaporación; una condición indicativa, un tanto desagradable, sino también es una amenaza para la vida. La humedad relativa es generalmente un indicativo importante de la razón de transpiración y pérdida de calor en plantas y animales.
A principios de junio del 2008 en el Puerto de Veracruz, la temperatura fue un poco mayor a 40ºC, y una humedad relativa cerca del 50%, lo que provocó una Temperatura Aparente muy cerca de los 50ºC, falleciendo personas adultas y un deportista en la playa. Ver cuadro superior.
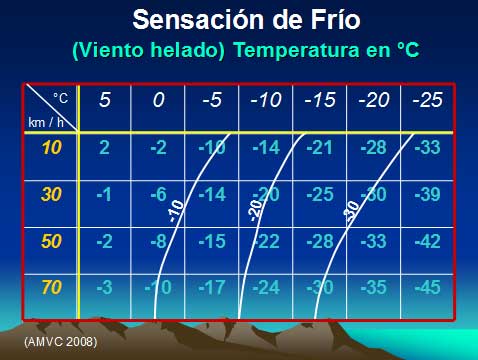
Sensación de Frío


Un viento continuo provoca que uno sienta más frío a lo esperado o supuesto. La evaporación tiene un efecto de enfriamiento, a mayores vientos la transpiración es mayor y el sudor se evapora de la piel, dejando que uno se sienta helado hasta los huesos.
Sensación de Frío
¿Por qué sentimos? ¿Tanto calor o tanto frío?
Bibliografía
- Benenson, W., Harris, J. W., Stocker, H. and Lutz, H.
2002 Handbook of PHYSICS. Springer-Verlag New York, Inc. - Burroughs, W. J., Crowder, B., Robertson, T., Vallier-Talbot, E., Whitaker, R.
1998 Observar el Tiempo. Weldon Owen Pty Limited 1996.
Editorial Planeta S.A. - Douglas, Paul.
2004 Restless Skies. Barnes & Noble Publishing
122 Fifth Avenue, New York. - Eden, P. and Twist, C.
1995 Tiempo y Clima. Dorling Kindersley Ltd., Londres - Emilsson, Ingvar.
1971 Elementos de oceanografía física. Universidad Nacional
Autónoma de México. México, DF. - Hess, S. H.
1959 Introduction to Theoretical Meteorology.
FloridaStateUniversity. Holt, Rinehart and Winston, New York. - Lutgens, F. K. and Tarbuck E. J.
2004 The atmosphere, an introduction to Meteorology. Ninth Edition.
Prentice Hall. Upper Saddle River, New Jersey07458. - Williams, Jack.
1997 The Weather Book. Second Edition. Vintage Books.
A division of Random House, Inc. New York.











Artículos Relacionados: